 Химия
: задал sanjanadevaraj26
Химия
: задал sanjanadevaraj26  Химия
Химия BaSO4+H2SO4=Ba(HSO4)2
n = m/M M(H2SO4)= 2+32+16*4 = 98г/моль
n(H2SO4) = 85.5г / 98 г/моль = 0,9 моль
n(Ba(HSO4)2) = 0,9 моль
m = n*M M(Ba(HSO4)2) = 331г/моль
m(Ba(HSO4)2)= 0,9 *331 = 297,9 г
ответ:m(Ba(HSO4)2)= 0,9 *331 = 297,9 г
 Химия
Химия Н2S + 2K = K2S + H2 ( выделяеться)
K2S+Pb(NO3)2=2KNO3+PbS
 Химия
Химия 2NaH + O2 = 2NaOH
P2O5 + 3Na2O = 2Na3PO4
 Химия
Химия если при нагревании кристаллогидрата вес уменьшается на 5,4 г, это - вода, а
36,6-5,4=31,2г - масса соли
ВаСІ2*хН2О
М(ВаСІ2)=208
М(Н2О)=18
31,2г 5,4г
208г 18х
х=208*5,4/31,2*18=2
формула ВаСІ2*2Н2О
 Химия
Химия 14,15 и 209 - это нуклонные числа или просто общее количество протонов и нейтронов(нуклонов) в ядре данного изотопа(элемента).А порядковый номер - это протонное число,или количество протонов в ядре.Поэтому разница между нуклонным числом(общим количеством частиц в ядре) и протонным числом(количество протонов) есть количеством нейтронов:
азот-14 имеет в ядре 7 протонов и (14-7) 7 нейтронов;
азот-15 - 7 протонов и (15-7) 8 нейтронов
висмут-209 - 83 протона и (209-83) 126 нейтронов
 Химия
Химия Химическая формула сахарозы С12Н22О11. Молярная масса = 343,3 г/моль. 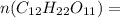
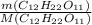 .
. 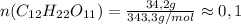 моль
моль
 Химия
Химия масса теор(СО2) = 40/0.9091 = 44г
n(CO2) = 1 моль
х 1моль
Ca2CO3 = CO2 + СаО
1моль 1моль
х=1моль
m(Ca2CO3) = 1*100=100г
 Химия
Химия Ba(OH)2+H2SiO3=BaSiO3+2H2O
Ba(OH)2+Na2SO4=BaSO4+2NaOH
Ba(OH)2+SO2=BaSO3+H2O
3Ba(OH)2+P2O5=Ba3(PO4)2+3H2O
Ba(OH)2+SiO2=BaSiO3+H2O
 Химия
Химия 2NH3 + H3PO4(избыток) ---> (NH4)2HPO4- гидроортофосфат аммония
NH3 + H2PO4(недостаток) ---> (NH4)3H2PO4-ортофосфат аммония
 Химия
Химия HNO3+NH3=NH4NO3
M(NH4NO3)=80г/моль
n(NH4NO3)=320/80
n(NH4NO3)=4моль
n(NH4NO3)=n(HNO3) - за уровнением
M(HNO3)=63г/моль
m=n*M
m=4*63
m=252г - чистой азотной кислоты.
Тогда масса раствора будет 252/0,1=2520г
ответ: 2520г 10% раствора азотной должна быть введена во взаимодйствие с аммиаком для получения 320г нитрата аммония.







